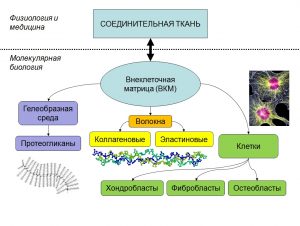
Составляя около 50% массы тела, соединительная ткань(СТ) является одним из четырех основных типов ткани (в дополнение к эпителиальной,мышечной и нервной ткани). Основная функция СТ – это структурная поддержка всех других тканей. Хрящ и кость являются основными разновидностями соединительной ткани. Недифференцированная дисплазия соединительной ткани (нДСТ), связанная с абнормальными структурными и функциональными изменениями CT, стимулирует развитие хронических патологий. Клинико-морфологические проявления нДСТ необычайно разнообразны и включают скелетные изменения, связанные с нарушением строения хряща, непропорционально длинные конечности, арахнодактилию, деформации грудной клетки, сколиозы позвоночника, плоскостопие, патологию развития зубов, прикуса, кисты, патологию суставов (склонность к вывихам), гиперэластичность и склонность к травматизации кожи, расширение вен и внешние признаки ускоренного старения (раннее формирование морщин, деформация овала лица, гравитационный птоз). Кроме того, нДСТ предрасполагает к бронхолегочным и реноваскулярным патологиям, способствует потере мышечной мас сы (в том числе сердечной и глазодвигательной мускулатуры). Поражения сердечно–сосудистой системы весьма разнообразны: пролапс митрального клапана, венозная недостаточность, варикозная болезнь, патологии гемостаза [1-3]. Самые различные микроэлементы играют существенную роль в поддержании структуры и функции СТ [4-10].
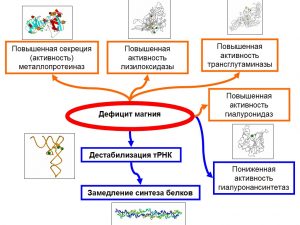
Магний является одним из наиболее важных для СТ микроэлементов. Именно при достаточной обеспеченности магнием достигается баланс между активностями коллагеназ и эластаз, деградирующих волокна коллагена и эластина и активностью биосинтетических ферментов СТ, в т.ч. ферментов биосинтза глюкозаминогликанов (гиалуронансинтетаз, гиалуронидаз, галактозидаз). . Напротив, при дефиците Mg2+синтез белков в соединительной ткани замедляется, внеклеточная матрица прогрессивно деградирует, так как структурная поддержка ткани (в частности, коллагеновые волокна) разрушается быстрее, чем синтезируется. Наиболее вероятными механизмами действия магния являются 1) дестабилизации тРНК и сплайсеосом; 2) деактивация гиалуронансинтетаз и повышение активности гиалуронидаз; 3) активация матричных металлопротеиназ; 4) инактивация эластаз; 5) активация трансглутаминазы и лизилоксидазы, а также 6) аутоиммунные реакции,обусловленные аллелем bw35 гена HLA–B. Компенсация дефицита магния полезна при дегенеративных заболеваниях позвоночника [2], для поддержки нормальной пигментации и других показателей состояния кожи [3], для ускорения ранозаживления и повышения качества рубца [4].
Рис. Механизмы, связывающие дефицит магния со структурой соединительной ткани.
В эксперименте, прием органической соли магния позитивно отразился на течении восстановительного процесса в коже. Склеротические изменения СТ в зоне повреждения у животных, получавших препарат магния, на 30–й день оказались выраженными в меньшей степени, чем в контрольной группе. Применение оротата магния достоверно сокращало сроки полного завершения эпителизации ран, предотвращало избыточное разрастание коллагеновых фибрилл на фоне стимулирования роста эластиновых волокон, придающих эластичность рубцу, роста числа фибробластов СТ и формирования аморфного вещества, что способствует повышению качества рубца [4].
По данным эпидемиологических исследований, дефицит магния – один из наиболее широко распространенных нутриентных дефицитов среди россиян, что не может не сказаться на качестве протекания беременности. Состояние соединительной ткани в достаточно существенной степени влияет на течение и исход беременности, так как она образует «опорный каркас» для всех тканей и органов. Недостаток магния сопряжен с широким спектром осложнений беременности и родов: повышением тонуса миометрия, преждевременными родами, преэклампсией и эклампсией, артериальной гипертонией беременных, аритмией и мышечными судорогами беременных, избыточной прибавкой массы тела, гестационным диабетом и метаболическим синдромом в послеродовом периоде и др. [5-10]. Применение современных методов интеллектуального анализа данных позволило установить комплексные и зачастую неочевидные для врача взаимосвязи между различными проявлениями ДСТ и осложнениями беременности и родов. Дефицит магния способствует развитию плацентарной недостаточности (ПН) с 12-кратным увеличением количества случаев задержки развития плода у беременных основной группы [7], что подтверждается результатами морфологического и иммуногистохимического исследования плаценты и пуповины. Исследование позволило установить комплексные взаимосвязи между проявлениями нДСТ, дефицитом магния, осложнениями беременности, родов и результатами исследования последов [8].
Кальций, магний, витамины B2, B6, C и E способствуют профилактике краниостеноза (от лат. cranium – череп, syn – вместе, ostosis – связанный с костью) – патологического состояния соединительной ткани новорожденного, при котором один или более черепных швов ребенка преждевременно минерализуется, меняя тем самым возможные направления роста черепа [5] (т.н. “преждевременное закрытие родничков). Активность сигнальных каскадов, непосредственно связанных с заращиванием черепных швов (сигнальные каскады ФРФ, трансформирующего фактора роста b2, интерлейкина-11), зависит от ряда этих и других микронутриентов. Дефициты магния, цинка, кальция, инозитола и холина будут приводить к нарушениям регуляции этих сигнальных каскадов и, следовательно, к нарушениям развития костной ткани – абнормально ускоренной оссификации (краниостеноз) или, наоборот, крайне замедленной оссификации (рахит). Особо следует отметить роль ФРФ-23, который необходим для регуляции реадсорбции кальция, фосфата и активных форм витамина D в почках [5]. Коррекция дефицита кальция также имеет важное значение для профилактики нарушений метаболизма костной ткани, кожи, волос [9-11]. Изучение влияния комбинированного средства, содержащего кальций, витамин D3 и остеотропные минералы, на регенерацию костной ткани у крыс с переломом малоберцовой кости показало, что в группе крыс, получающей данное средство, регенерация кости идет быстрее и качественнее. [12]
На структуру соединительной ткани существенно влияют железо и его синергисты, в т.ч. медь и марганец. Эти три элемента оказывают синергидное воздействие на эффективную компенсацию ЖДА, что весьма важно для выживания фибробластов и других типов клеток, синтезирующих компоненты и поддерживающих структуру СТ. Специфические эффекты воздействия железа и меди на СТ включают синтез и сборку коллагена (образование поперечных сшивок коллагеновых полипептидов), а марганца – синтез глюкозаминогликанов, образующих гелеобразную основу СТ [6]. В исследовании [13] установлен комплекс взаимосвязей между обеспеченностью плаценты железом, медью и марганцем и гистологическим строением плаценты, найдено влияние дефицитов микроэлементов на течение беременности у пациенток с нДСТ. В основную выборку были включены беременные с НДСТ (n = 47), средний возраст 29 ± 6 лет. Установлены взаимосвязи между состоянием беременных с ДСТ и анемией, а также содержанием железа, меди и марганца в тканях плаценты. Наиболее высокие показатели железа, меди и марганца в плаценте, соответствующие верхним квартилям содержания этих микроэлементов, были достоверно ассоциированы с меньшим количеством осложнений беременности, родов и патологических изменений плаценты. В частности, у женщин этих групп не отмечались такие особенности состояния плаценты, как фибриноидный некроз (р = 0,00005), аномалии сосудов плаценты и пуповины (р = 0,001), преждевременная отслойка нормально расположенной плаценты (ПОНРП, р = 0,04), гиперплазия и гипоплазия плаценты (р < 0,05). При родоразрешении данной группы пациенток не возникло показаний к проведению операции кесарева сечения (р < 0,041); состояние детей при рождении было удовлетворительным (оценка по шкале Апгар не менее 9 баллов, р < 0,001) [13].
Литература
- Торшин И.Ю., Громова О.А. Дисплазия соединительной ткани, клеточная биология и молекулярные механизмы воздействия магния. РМЖ. 2008. Т. 16. № 4. С. 230-238.
- Гоголев А.Ю., Керимкулова Н.В., Егорова Е.Ю., Волков А.Ю., Торшин И.Ю., Громова О.А. Рандомизированное исследование эффективности магния оротата в комплексной программе реабилитации пациентов, перенесших операцию по удалению грыжи межпозвоночного диска. Фарматека. 2012. № 9 (242). С. 69-75.
- Торшин И.Ю., Громова О.А. Систематический анализ молекулярных механизмов участия магния в регуляции пигментообразования кожи. РМЖ. 2012. Т. 20. № 22. С. 1142-1149.
- Суракова Т.В., Жидоморов Н.Ю., Гришина Т.Р., Кодин А.А., Чибисов И.В., Илларионова Е.Э., Коробова О.Р., Торшин И.Ю., Лепахина Л.Э., Громова О.А. Влияние оротата магния на регенерацию кожи. РМЖ. 2012. Т. 20. № 11. С. 575-581.
- Торшин И.Ю., Громова О.А., Сухих Г.Т., Сотникова Н.Ю. Молекулярные роли микронутриентов в физиологических механизмах закрытия родничков и профилактика краниостеноза. Гинекология. 2012. Т. 14. № 5. С. 60-67.
- Керимкулова Н.В., Торшин И.Ю., Громова О.А., Cеров В.Н., Никифорова Н.В. Систематический анализ молекулярно-физиологических эффектов синергидного воздействия железа, марганца и меди на соединительную ткань. Гинекология. 2012. Т. 14. № 6. С. 51-60.
- Керимкулова Н.В., Никифорова Н.В., Владимирова И.С., Торшин И.Ю., Громова О.А. Влияние недифференцированной дисплазии соединительной ткани на исходы беременности и родов. комплексное обследование беременных с дисплазией соединительной ткани с использованием методов интеллектуального анализа данных. Земский врач. 2013. № 2 (19). С. 34-38.
- Керимкулова Н.В., Серов В.Н., Никифорова Н.В., Торшин И.Ю., Громова О.А., Перетятко Л.П., Кузнецов Р.А. Влияние недифференцированной дисплазии соединительной ткани на исходы беременности и родов: клинические аспекты, морфологические и иммуногистохимические особенности плаценты. Земский врач. 2013. № 3 (20). С. 28-31.
- Громова О.А., Торшин И.Ю., Пронин А.В., Гришина Т.Р., Семенов В.А. Значение кальция для здоровья кожи, волос и ногтей и вопросы рациональной коррекции его потребления. Русский медицинский журнал. Медицинское обозрение. 2014. Т. 22. № 24. С. 1796-1799.
- Керимкулова Н.В., Никифорова Н.В., Сонина Н.П., Перетятко Л.П., Торшин И.Ю., Кузнецов Р.А., Громова О.А. Влияние цитрата магния на течение беременности при дисплазии соединительной ткани. Гинекология. 2013. Т. 15. № 5. С. 76-82.
- Громова О.А., Торшин И.Ю., Лиманова О.А. Кальций и его синергисты в поддержке структуры соединительной и костной ткани. Лечащий врач. 2014. № 5. С. 69.
- Громова О.А., Торшин И.Ю., Демидов В.И., Жидоморов Н.Ю., Сотникова Н.Ю., Волков А.Ю. Роль остеотропных минералов в профилактике и комплексном лечении перелома берцовой кости: результаты рандомизированного плацебо-контролируемого эксперимента. Лечащий врач. 2014. № 11. С. 89.
- Керимкулова Н.В., Никифорова Н.В., Торшин И.Ю., Гоголева И.В., Волков А.Ю., Громова О.А. Беременность и роды у женщин с дисплазией соединительной ткани и железодефицитной анемией. Вопросы гинекологии, акушерства и перинатологии. 2014. Т. 13. № 5. С. 11-21.
